「脳ドレナージ」でアルツハイマー病を予防する方法
「脳ドレナージ」でアルツハイマー病を予防する方法
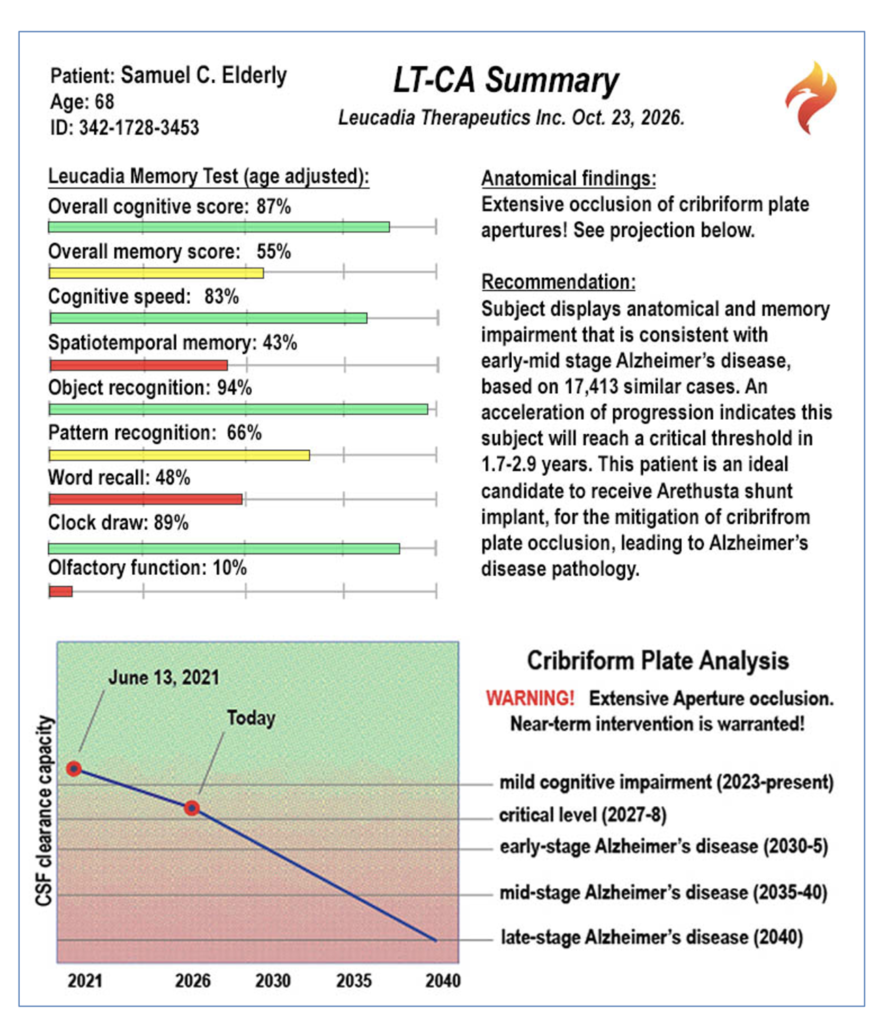
Leucadia Therapeutics は、篩状板の脳脊髄の「頭脳流出」を修復し、病気を予防する埋め込み型デバイスをテストします。
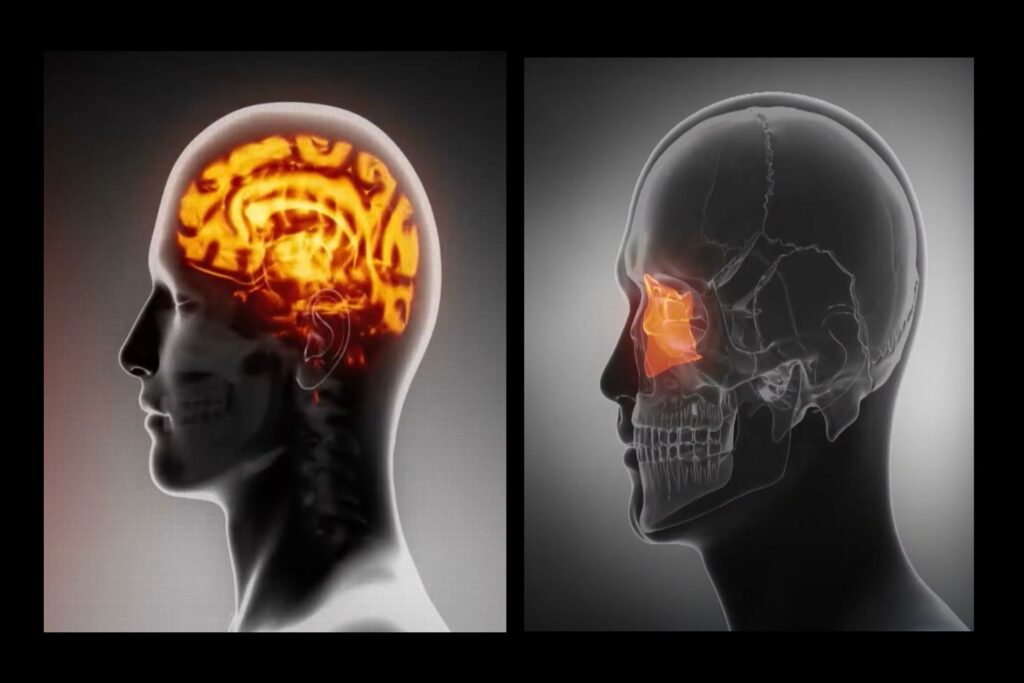
「XNUMX年からXNUMX年で認知症やアルツハイマー病を発症することを誰かに伝えることと、具体的な解決策を提供することは別のことです.」 これは、Leucadia Therapeutics 社の創設者兼 CEO である Doug Ethell の厳しい言葉です。
過去 XNUMX 年間、アルツハイマー病の研究者は、アルツハイマー病と認知機能の低下が、タウタンパク質のもつれの蓄積と並行して、脳内のベータアミロイド斑の増加と関連していることを発見しました。臨床試験、その多くは失敗に終わりました。
2014 年、神経科学者の Doug Ethell は、アルツハイマー病および関連する認知症の引き金に関する新しい仮説を発表しました。 しかし、それだけではありません。2015 年に、彼は自分の仮説に基づいた治療法を開発するために Leucadia Therapeutics 社を設立しました。
彼の研究は、プラークともつれが、これらの病理学的特徴の形成を引き起こす、より深刻な基礎疾患の影響であることを示しています.
5 年 2021 月 XNUMX 日、エセル博士のチームは、彼の仮説を裏付ける XNUMX つの研究について報告しました。 アルツハイマー病の病因に極めて重要な役割を果たしている「Cribriform Plate を介した CSF Egress の障害」というタイトルの原稿は査読中であり、「MedRXiv」のプレプリント サーバーで利用できます。生命科学に関する電子形式 (医学、臨床研究、および関連する健康科学の分野で、完全ではあるが未発表の原稿を読者に無料で配布します)。
この研究は、アルツハイマー病の診断、治療、予防に影響を与え、篩板板の老化が疾患の病因に重要な役割を果たしているという決定的な証拠を提供します。 これらの発見は、認知症やアルツハイマー病が不可逆的になる何年も前に病気を予測し、治療するための新しい機会への扉を開きます。
この記事は、アロイス アルツハイマーによって発見された病気を予防するためにロイカディアによって開発された埋め込み型デバイスに関するものです。 このデバイスは 2022 年に臨床試験に入る予定です。平均余命が延びるにつれて、彼のデバイスはペースメーカーと同じくらい一般的なものになると Doug Ethell は考えています。
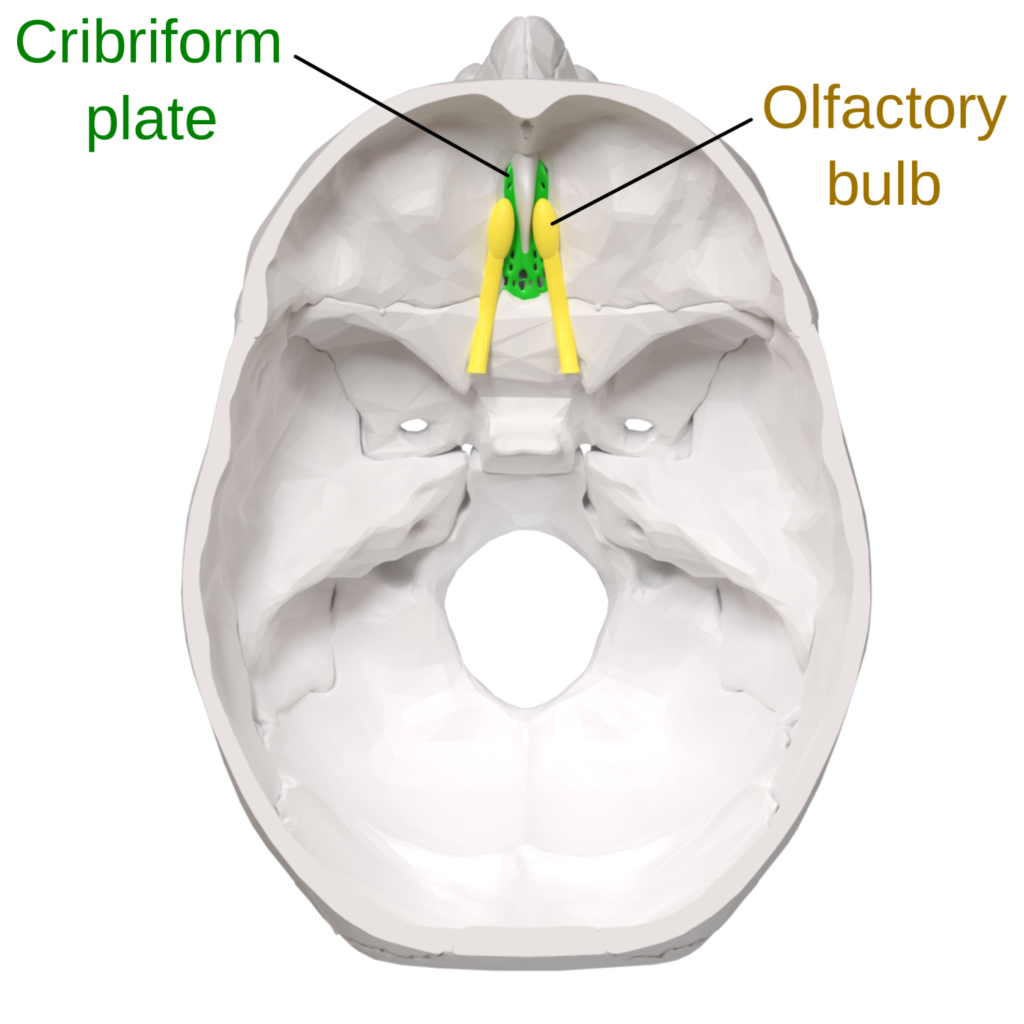
篩状板の骨化による脳への影響
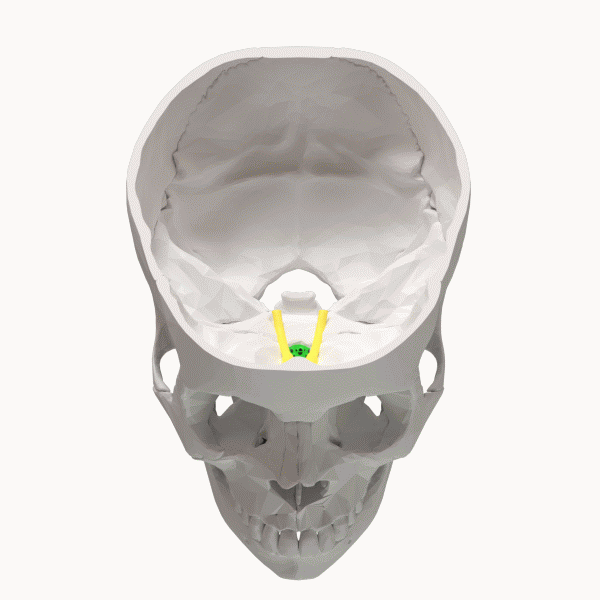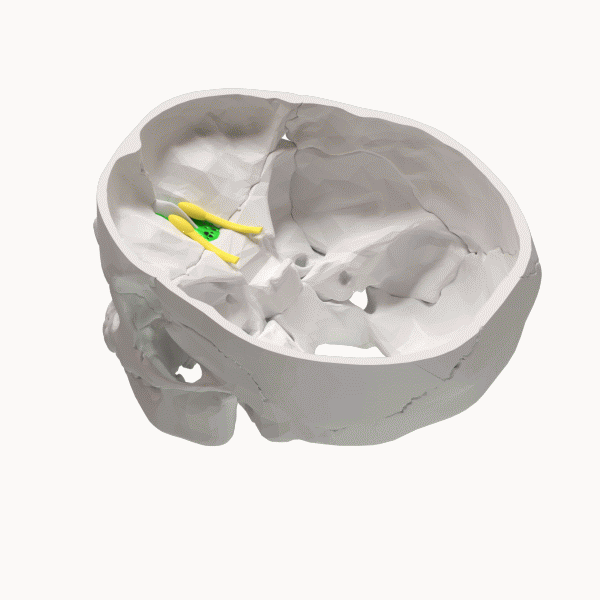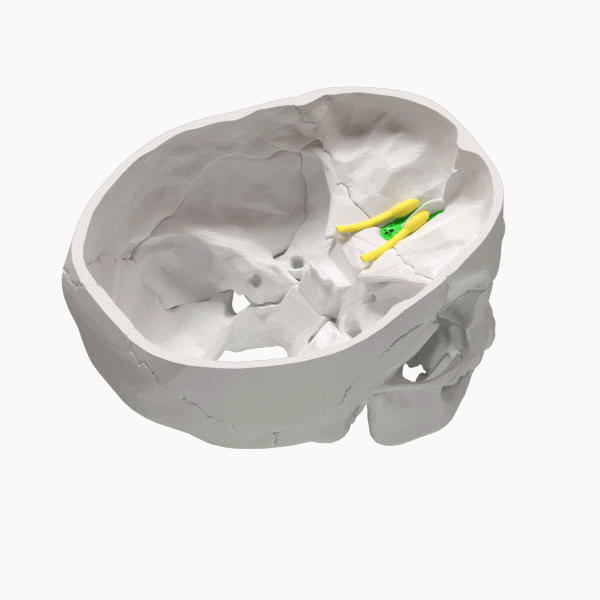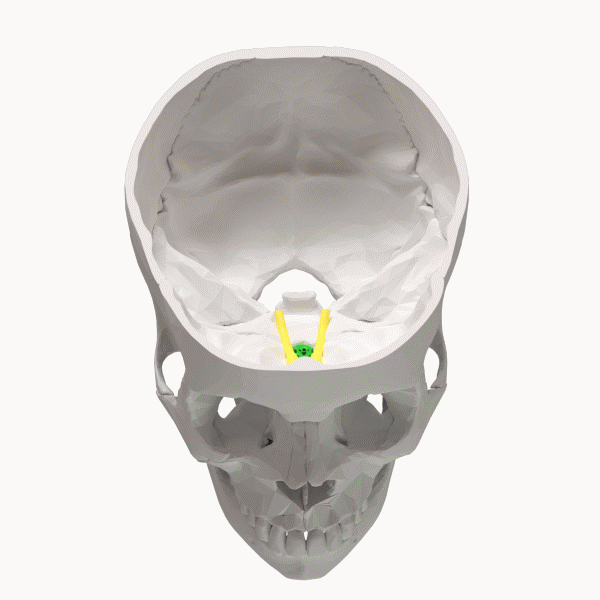
篩骨板は、鼻腔の上部に位置する多孔質の骨構造です。 プレートには、窩と呼ばれるXNUMXつの深いポケットと、嗅孔と呼ばれる多くの穴があります。 これらの穴を通って、においを伝える嗅神経が通過します。
篩状板は、脳が廃棄物を脳脊髄液 (CSF) に排出するために使用する流出経路です。 脳は毎日約 XNUMX リットルの脳脊髄液を生成しますが、その約 XNUMX 分の XNUMX しか篩板から排出されません。
しかし、その少量の脳脊髄液は、新しい記憶を作り、世界で私たちを方向付ける鍵となる脳領域をきれいにする役割を果たしています. 年齢とともに、篩状板は骨化し、多孔性が低下します。
小さな穴が塞がり、脳脊髄液の流れが制限されます。 この液体が脳から排出される量が少なくなると、記憶を司る脳の最上部領域に老廃物や毒素が蓄積します。
これらの老廃物は、アルツハイマー病の XNUMX つの重要な特徴であるプラークが形成され、ニューロンがもつれを形成する「スラフ」(死んだ組織の領域) を形成します。
Doug Ethell による研究は、この疾患が篩状板を通る脳脊髄液の排出障害に起因することを示しています。
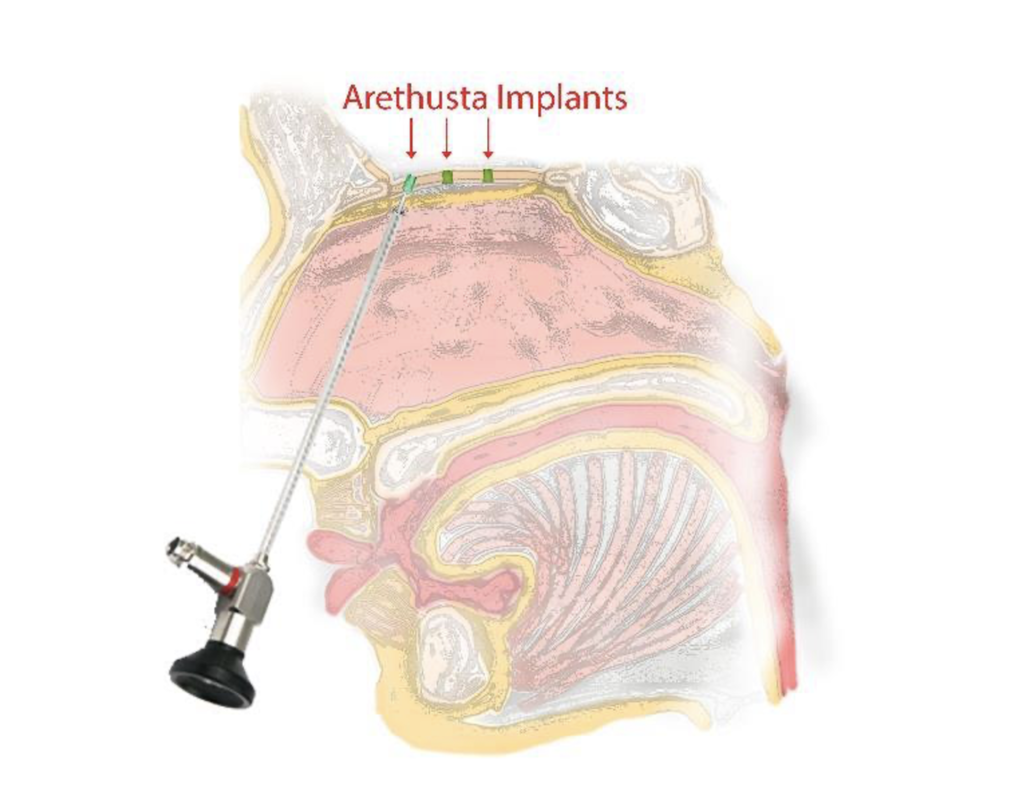
初期のアルツハイマー病を攻撃するための脳脊髄液手術
脳脊髄液 (CSF) は、リンパ系が体の残りの部分から毒素やその他の不純物を取り除くのと同様に、脳の細胞間スペースから有毒な代謝物を取り除きます。
アルツハイマー病に冒された脳の最初の領域は、篩状板を通って流出する脳脊髄液によって除去されるため、その構造に影響を与える要素は認知症のリスクを高める可能性があります.
篩状板の閉塞を加速し、それらの脳領域からのCSF媒介クリアランスを減少させる老化およびライフイベントは、プラークおよびもつれの形成を含むアルツハイマー病のリスクを増加させる.
Leucadia Therapeutics は、2022 年の臨床試験の準備を進めています。この臨床試験では、植込み型デバイスを使用して、篩状板を通る CSF 排液を回復させ、アルツハイマー病を予防します。
Ethell 博士は、平均余命が延びるにつれて、彼のデバイスがペースメーカーと同じくらい一般的になるだろうと考えています。 この十分に根拠のあるアプローチは、初期の軽度認知障害を逆転させ、アルツハイマー病の発症を完全に防ぐはずです.
Leucadia の特許取得済みの Arethusta 技術は、篩状板を通る CSF の流れを回復させ、アルツハイマー病に冒された初期の脳領域からの毒性代謝産物の除去を強化します。
圧力の問題? 私たちは皆それらを持っていますが、ルールはほとんどありません…
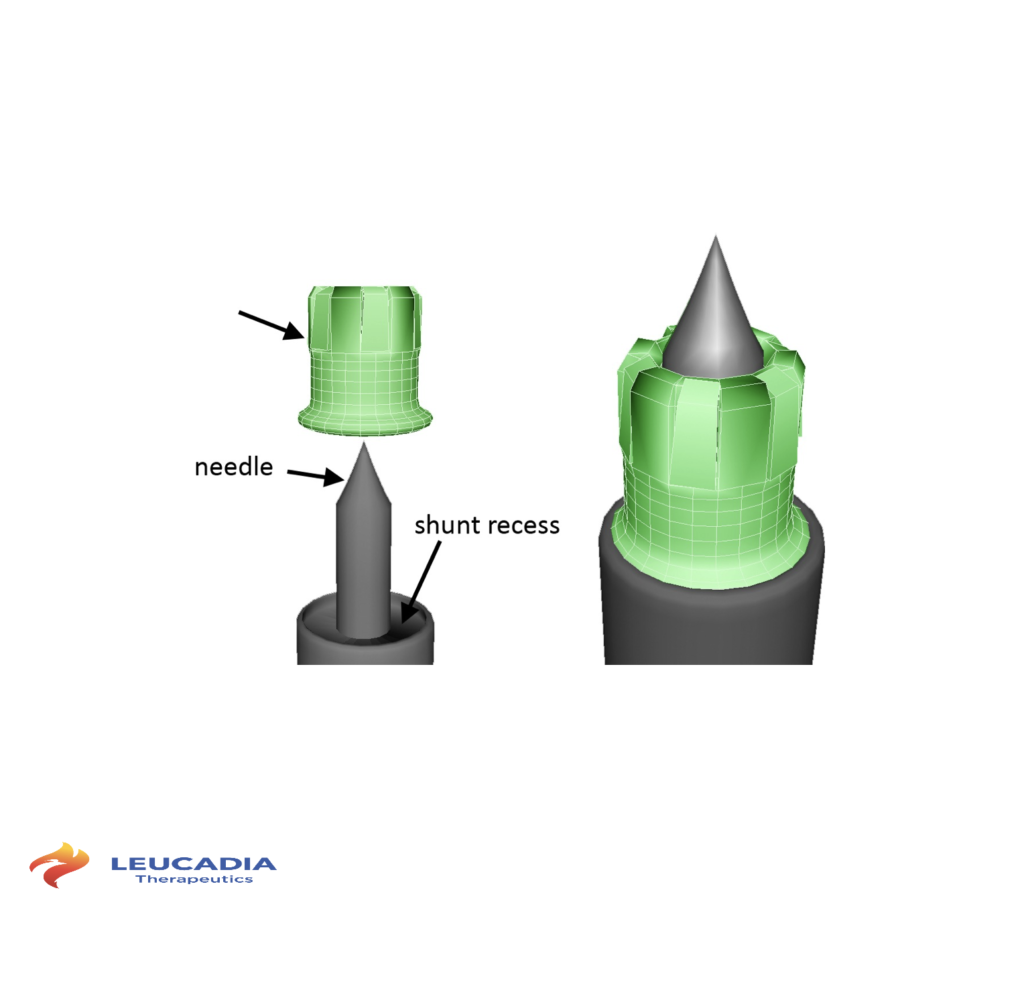
アレトゥーサという名前は、ギリシャ神話に登場する水の妖精で、アルテミスが彼女を隠された地下の小川に変えて救ったことに基づいています。 Leucadia のデバイスは、組織の下にチャネルを作成し、脳から液体を排出します。
鼻腔の上部に篩骨板があるため、アレスタスタ装置は鼻から導入されます。 フェレットの臨床研究では、研究者はプレートからの排水を人為的にブロックしました。
その閉塞は、アルツハイマー病が最初に発症したのと同じ脳領域で、認知障害と萎縮を誘発しました。
Arethusta は、アルツハイマー病が「始まる」脳の領域から脳脊髄液を介した老廃物除去を回復します。
水頭症の CSF のシャント管理は脳神経外科医によって毎日行われますが、Arethusta はより具体的な効果のために非常に異なる場所から CSF を吸引します。
「CT スキャンは 3.000 ~ 65.000 レベルのグレーを生成しますが、人間の目は 20 階調未満しか識別できず、大きな 3D ボリュームを手動でセグメント化することは難しく、時間がかかります。 Leucadia が開発した AI アルゴリズムは、低線量のコーンビーム CT スキャンを使用して、エッジ、境界、穴を特定し、開口部が発生した場所とその大きさを明らかにします。」
メタボリックシンドロームとは? そして、どうすればそれを防ぐことができますか?

ふるい板の形態変化を調べる「深層学習」
ロイカディア・セラピューティクス は、研究者が膨大なデータセットを分析できるようにする人工知能アルゴリズムを開発しました。
この新しいアプローチには、超解像度コントラスト マイクロ CT の高度な手法に適用される最先端のディープラーニング、新しい動物モデル、および機械学習用に高度に精選されたデータを生成するように設計された大規模な臨床研究が組み込まれています。
Leucadia の科学者は、これらの方法を組み合わせて、アルツハイマー病における篩状板の形態の変化を比較しました。
甲状腺炎と甲状腺腫:これがベルガモ地域で人々が病気になる方法です
新しいアプローチは、XNUMX つの異なる手順を効果的に組み合わせたものです。
1) 高解像度のマイクロ CT とディープ ラーニングを使用して、死後の被験者から分離された篩骨サンプルを評価しており、その多くは AD と診断されています。
この人間の篩板の病理学的分析は、誰も存在を知らなかった流域の発見につながり、脳脊髄液が篩板からどのように排出されるかを詳しく説明しました。
2) 研究者は、CP 開口部閉塞の行動および病理学的影響をテストするために、新しいフェレット モデルを開発しました。
フェレットのモデルはふるい板をふさぎ、アルツハイマー病によって最初に影響を受けた脳の領域の記憶喪失と萎縮を引き起こしました。
3) 研究者は、560 歳から 20 歳までの 95 人のボランティアのグループで、Leucadia の新しい認知テスト プラットフォームと篩板のコーン ビーム スキャンを使用して、篩板の老化と認知を評価しました。
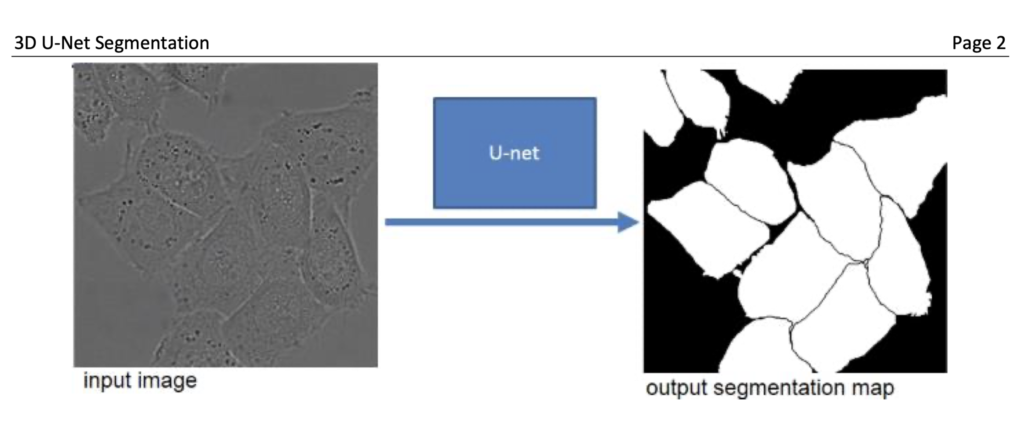
コンピューター断層撮影スキャンの 3D U-Net セグメンテーション
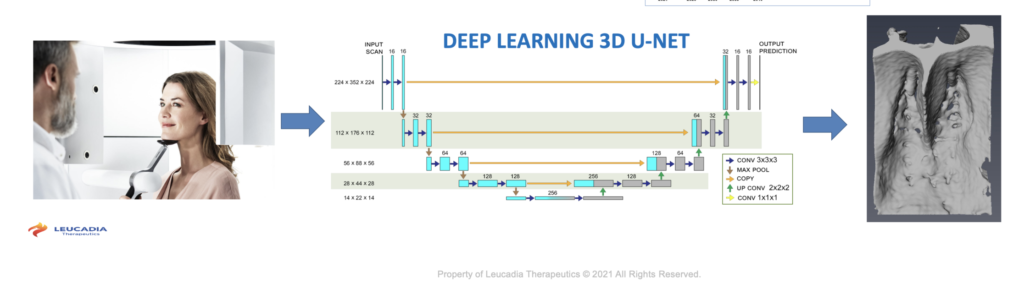
3D U-Net セグメンテーションは、畳み込みニューラル ネットワーク ベースのアーキテクチャであり、通常はラベルの分類に使用されます。 ただし、3D 医用画像では、U-Net は分類以上のことができます。
各ピクセルのクラス ラベルを予測するためのローカリゼーションが含まれており、そのピクセルの周囲の局所領域を入力として提供します。
機械学習アルゴリズムは、ボクセルを正規化された浮動小数点計算として扱うため、65.000 レベルのグレー スキャンでエッジと境界を表すボクセルの組み合わせを正規化して、解像度が劣るコーンビーム CT の骨構造を予測できます。
Doug Ethell と彼のチームは、3D-UNet を使用して、死後のマイクロ CT サンプルからの非常に高解像度のサンプルでモデルをトレーニングしました。

次に、これらのモデルを使用して、解像度の低い低線量臨床 CT スキャンから骨パターンを予測しました。 この画像は 20 秒のコーンビーム CT スキャン画像であり、骨の細部が見えにくいことに注意してください。 情報はそこにありますが、何千ものグレー レベルに分散しています。
右側の画像は、「トレーニングされた」AI モデルが左側のスキャンからどのように骨を予測したかを示しています (開口部を含む詳細に注意する必要があります)。
CT スキャナーは 3.000 レベルのグレーを生成しますが、人間の目で識別できる階調は 20 未満であり、手動によるセグメンテーションは困難で時間がかかります。
Leucadia が開発した AI アルゴリズムは、低線量のコーンビーム CT スキャンを使用して、エッジ、境界、穴を特定し、開口部が発生した場所とその大きさを明らかにします。
FDA の次のステップと 2022 年のシリーズ A 資金調達
この作業は、2022 年に開始されるアレススタの臨床試験のための食品医薬品局への Leucadia の申請の基礎を築きます。
現在の投資家には、David Gobel、Jim Mellon、Methuselah Fund、Methuselah Foundation が含まれます。 同社は、Arethusta の臨床試験に資金を提供するために、2022 年にシリーズ A の資金調達を計画しています。
出典:「篩状板を介したCSF排出の障害は、アルツハイマー病の病因において頂点の役割を果たす」

あなたも興味があるかもしれません:
若者と暗号通貨: ビットコインについてもっと知るには…
子どもたちにデジタル通貨やブロックチェーンを紹介することは、子どもたちのテクノロジーやイノベーションへの親近性を考えると、刺激的な取り組みになる可能性があります。
「患者が中心」:大きな希望と上院での会合
ヨーロッパの医療における医療機器のイノベーションの重要性というテーマが、15月XNUMX日にローマで専門家と政治家によって検討される予定
アルベルト・ニコリーニdistrictbiomedicale.it、BioMed News、Radio Pico の編集者




